Producción porcina en sistemas al aire libre: prevalencia de parasitosis en áreas rurales de Buenos Aires, Argentina.
Vet. Arg. – Vol. XXXVI – Nº 380 – Diciembre 2019.
Florencia Algañaraz1; Natalia Cardillo 2; Marco Matassa1; Raúl Sciarrotta1; Nicolás Tosonotti1; Graciela Vidales13
Resumen
El objetivo del trabajo fue determinar las prevalencias de helmintos gastrointestinales en establecimientos de producción de cerdos al aire libre en áreas rurales de la provincia de Buenos Aires, Argentina, fueron analizadas por el método de Mc Master modificado 251 muestras de materia fecal procedentes de veinticuatro establecimientos. La prevalencia de helmintos gastrointestinales fue de 65,3 % de las muestras analizadas. Las cerdas lactantes presentaron los valores de huevos por gramo de materia fecal (hpg) más elevados, aunque no hubo diferencias entre categorías (p>0.05). Los Trichostrongylideos fueron los parásitos de mayor prevalencia general y en las categorías cerdas lactantes y lechones de recría, siendo esta ultima la más parasitada (p<0.05). En cerdas gestantes la prevalencia de Ascaris suum fue mayor (p<0.05). Sobre el total de muestras de las categorías analizadas, el 40% resultaron positivas a coccidios y si bien los porcentajes fueron mayores en cerdas gestantes y lactantes (40,6 y 58,7% respectivamente), no hubo diferencias. El hallazgo de elevada prevalencia de parasitosis, los valores de hpg y, las infecciones mixtas de especies, confirman la importancia de establecer estrategias de prevención y control de las parasitosis para evitar pérdidas económicas, mejorar los índices de eficiencia y minimizar la generación de resistencia a drogas de uso frecuente en estos sistemas de producción.
Palabras clave: helmintos, coccidios, cerdos, producción al aire libre.
Swine production in outdoor systems: prevalence of parasitosis in rural areas of Buenos Aires, Argentina.
Summary
The objective of the work was to determine the prevalence of gastrointestinal helminths in outdoor pig production establishments, in rural areas in the province of Buenos Aires, Argentina, analyzed by the Mc Master method modified 251 fecal samples from twenty-four establishments. The prevalence of gastrointestinal helminths in the samples analyzed was of 65.3%. The lactating sows presented the highest values of eggs per gram of fecal matter (hpg), although there were no differences between categories (p> 0.05). Trichostrongylideos were the parasites of greater general prevalence and in the categories lactating sows and piglets, the latter being the most parasitized (p <0.05). In pregnant sows the prevalence of Ascaris suum was higher (p <0.05). Of the total samples of the categories analyzed, 40% were positive for coccidia and although the percentages were higher in pregnant and lactating sows (40.6 and 58.7% respectively), there were no differences. The finding of high prevalence of parasitosis, the values of epg and mixed species infections, confirm the importance of establishing prevention strategies and control of parasitosis to avoid economic losses, improve efficiency rates and minimize the generation of resistance to drugs of frequent use in these production systems.
Key words: helminths, coccidiosis, pigs, outdoor production
1 Universidad Nacional de Luján.
2 CONICET
13 Autor responsable. Departamento de Tecnología - Universidad Nacional de Luján (Buenos Aires, Argentina) Cruces rutas nacionales 5 y 7, 6700 Luján (Buenos Aires, Argentina)
[email protected]
Introducción
En Argentina, el 80% de las cerdas se encuentran en sistemas al aire libre (SAL), y el 20% en confinamiento. Una de las principales desventajas del sistema predominante es la pérdida de eficiencia a consecuencia de una mayor prevalencia de parasitosis, debido a menores condiciones higiénico-sanitarias y a la mayor posibilidad de acceso a hospedadores intermediarios, paraténicos o a cadáveres de animales silvestres que favorecen la transmisión y la perpetuación de los ciclos biológicos en el ambiente (Corwin y Straw, 2001). Los aspectos mencionados han sido indicados como los mayores factores de riesgo de la infección por helmintos y otros parásitos gastrointestinales, convirtiendo a los cerdos en reservorios de los mismos (Zewdneh et al, 2013).
Las nuevas tendencias sobre bienestar animal y la legislación de algunos países al respecto, impulsó cambios en los sistemas de producción (como el alojamiento de cerdas sueltas y en grupos) en condiciones similares a SAL o mixtos. Por otro lado, el auge de las producciones orgánicas supone menor uso de productos químicos (medicamentos, aditivos alimentarios) y mayor compromiso con el bienestar animal (Burden et al, 1987; Jensen y Svensmark, 1996; Carstensen et al, 2002). Se ha demostrado el resurgimiento de parásitos como el Oesophagostomum spp. y Strongyloides spp. debido a que estos sistemas favorecen las condiciones para la transmisión de parásitos y la supervivencia de sus formas infectantes (Thamsborg et al, 2010; Haugegaard, 2010; Roepstorff et al, 2011).
En diferentes estudios se han reportado los géneros y especies de parásitos de mayor prevalencia e impacto económico alrededor del mundo, identificando a Ascaris suum, Trichuris suis, Oesophagostomum spp., Trichinella spp., Strongyloides spp., Eimeria spp., Cystoisospora spp. y Cryptosporidium spp. (Nganga et al, 2008; Ngowi et al, 2014; Atawalna el al, 2015; Jufare et al, 2015) Macracanthorynchus hirudinaseus e Hyostrongylus rubidus, que predominan en animales criados en parcelas a campo, fundamentalmente por el hábito de hozar.
La disminución o pérdida de apetito, de la ganancia diaria de peso, de la conversión alimenticia y la predisposición a contraer otras enfermedades e incluso la muerte de los animales, son causa de importantes pérdidas económicas, en su mayoría subclínicas (Jufare et al, 2015). Por otro lado, las migraciones tisulares larvarias de nematodos como Ascaris suum, ocasionan lesiones en el hígado y pulmones de los cerdos desde edades tempranas que desvitalizan los tejidos, predisponen a enfermedades bacterianas secundarias y son causa de decomiso en los frigoríficos (Roepstorff et al, 2011). Muchas de estas parasitosis, además causan enfermedades zoonóticas, adquiridas por el hombre al consumir carne insuficientemente cocida o chacinados frescos, o por la ingestión de formas infectantes presentes en el ambiente. Recientemente, se ha demostrado el rol zoonótico de Ascaris suum y Trichuris suis, encontrándose infecciones mixtas con Ascaris lumbricoides y Trichuris trichuria en humanos y porcinos (Nejsun et al, 2005; Zhou et al, 2012; Nolasco et al, 2013).
En Argentina, la información epidemiológica y el impacto económico de las parasitosis en la producción porcina continúan siendo escasos, sobre todo en SAL. Es por ello que el objetivo del presente trabajo fue determinar las prevalencias de los helmintos gastrointestinales y de coccidios en cerdos a campo, en áreas rurales de los partidos de Luján, Mercedes y San Andrés de Giles de la Provincia de Buenos Aires (Argentina).
Materiales y métodos
Se elaboró una base de datos de establecimientos de pequeños productores y productores familiares de los partidos de Luján, Mercedes y San Andrés de Giles, de acuerdo a la estratificación del Servicio Nacional de Sanidad Animal y Calidad Agroalimentaria de Argentina (Senasa, 2016). Se muestrearon 24 establecimientos de producción porcina en sistemas al aire libre, dedicados a la producción y venta de lechones y con un número de madres de hasta 10 animales. Se obtuvo un total de 251 muestras de materia fecal (MF) de porcinos de distintas categorías, siendo muestreados al menos un 35% de animales por corral. La cantidad de muestras por establecimiento fue estimada por el método Scartec del programa Epi-Info® a partir de una prevalencia del 50% (estimada estadísticamente en función de la multiplicidad de factores determinantes de la ocurrencia de parasitosis y la escasez de antecedentes bibliográficos), N promedio de 15 animales por establecimiento, nivel de confianza 95%, error ≤ 0.05. Se identificaron los animales en forma individual y se tomaron muestras de MF estimulando la defecación por hisopado rectal. Las mismas fueron recolectadas en recipientes independientes, identificadas por número, categoría y establecimiento, y mantenidas a 4º C hasta su análisis. Se utilizó la técnica de flotación Mc. Master modificada para obtener el número de huevos por gramo de materia fecal (hpg). La identificación por género parasitario se realizó mediante observación por microscopía óptica de acuerdo a las características morfológicas y morfométricas de los huevos. La determinación de coccidios se realizó en forma cualitativa.
Las variables analizadas fueron, prevalencia general de parasitosis, específica por género parasitario y por categoría animal, estimadas como el cociente entre el número de muestras positivas y el número de muestras analizadas para cada caso. Los promedios de hpg en función de la categoría animal fueron analizados por test de ANOVA. Para el análisis de la prevalencia de cada género parasitario se utilizó el test de X2, para un nivel de significación estadística p<0.05. Los datos fueron analizados por el programa estadístico Statistix® versión 8.0.
Resultados y discusión
Sobre un total de 251 muestras de MF analizadas, la prevalencia de helmintos fue de 65.3 % (164/251), resultando positivos la totalidad de los establecimientos. En relación al análisis de los resultados por categorías de animales, las más poliparasitadas fueron cerdas gestantes y lactantes, y lechones de recría. En esta última categoría la prevalencia de helmintos gastrointestinales fue de 85.5 % (53/62) mayor que es resto de las categorías (p<0.05) (Tabla 1).
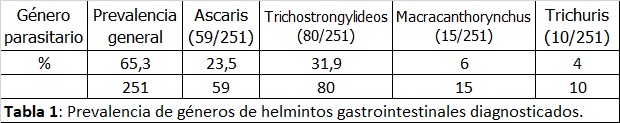

Figura 1
Los Trichostrongylideos fueron los parásitos de mayor prevalencia general (Figura I) específicamente en las categorías cerdas lactantes y lechones de recría (p<0.05); y Ascaris spp. en cerdas gestantes (p<0.05). Las cerdas lactantes fueron las que presentaron mayor carga parasitaria (647 hpg), si bien no hubo diferencias entre las categorías para este parámetro. Se identificaron ooquistes de coccidios en el 40% (100/251) de las muestras analizadas, en proporciones similares en las categorías positivas (Gráfico 1).
Las prevalencias de Trichuris y Macracanthorynchus no pudieron ser comparadas dado que en el análisis estadístico X2 los valores de las frecuencias esperadas fueron menores a 5 y menores a 2 en más del 20% de los casos.
La elevada prevalencia de helmintos y la frecuencia de infecciones mixtas detectadas en la totalidad de los establecimientos, y también a nivel individual, coinciden con trabajos previos publicados sobre parasitosis de cerdos en sistemas extensivos (Carstensen et al, 2002; Pinilla et al, 2005; Luna y Kyvsgaard, 2005; Eijck y Borgsteede, 2005; Nganga et al, 2008; Roesell et al, 2017; Ngowi el al, 2014). Estos autores indican que este nivel de parasitosis puede constituirse en una importante causa de pérdidas productivas, agravada por la aplicación incorrecta de drogas antiparasitarias en relación a la dosificación o espectro de acción. Específicamente, el 75% (18/24) de los productores de los establecimientos muestreados manifestaron desparasitar con avermectinas, dosificando al azar sin ningún tipo de asesoramiento ni plan estratégico, y tres de ellos no aplicaban tratamiento antiparasitario alguno. Estos aspectos, generalmente, no son tenidos en cuenta en sistemas de producción al aire libre y evidencian deficiencias en el manejo sanitario que explicarían, en parte, los resultados obtenidos.
Dadas las características de los establecimientos muestreados, no fue posible identificar a los lechones lactantes con sus respectivas madres, pero la elevada prevalencia de helmintos, valores de hpg y el poliparasitismo hallado en cerdas reproductoras, convertirían a las mismas en una importante fuente de infección para las crías, y refuerza la importancia de desparasitar a las hembras al ser trasladadas a las instalaciones de maternidad días previos a la fecha probable de parto.
El hallazgo de Trychostrongylideos en el 31.9 % y de Ascaris sp en el 23.5% de las muestras de MF de cerdas lactantes coinciden con los reportados por otros autores en diferentes partes del mundo (García Vallejo, 1999; Eijck y Borgsteede (2005); Zewdneh et al, 2013). En sistemas de producción de cerdos al aire libre en Argentina, la prevalencia de Ascaris suum coincide con lo reportado por Descarga et al (2010) (entre 0 a 21% en diferentes parcelas), pero son inferiores a lo hallado por Vazquez et al (1997) quienes registraron una prevalencia de 56.06%.
En Dinamarca se reportaron prevalencias elevadas de Ascaris suum para los animales de recría y engorde, y menores en cerdas reproductoras; Trichuris suis y Oesophagostomum spp. fueron reportados en menores proporciones para las mismas categorías mientras que la prevalencia de coccidios fue menor al 10% en cerdas reproductoras y animales de engorde (Carstensen et al, 2002), y en Venezuela, Pinilla et al (2005) al evaluar la presencia de parásitos en diferentes sistemas de producción halló mayores prevalencias en sistemas de cama profunda y a campo (43.5% y 23.4% respectivamente). En similares sistemas de producción, Luna y Kyvsgaard (2005) en Nicaragua y Eijck y Borgsteede (2005) en Holanda coincidieron en sus hallazgos y determinaron la presencia de Trichuris, Macracantorynchus, Oesophagostomum, Ascaris e Hyostrongilus en prevalencias elevadas, fundamentalmente para estos dos últimos parásitos y en cerdos adultos.
Se identificaron ooquistes de coccidios en el 40% (66/245) de las muestras analizadas, en proporciones similares en las categorías positivas (Cuadro 1). La prevalencia hallada en el presente estudio, coincide con reportes previos en SAL por Dalla Costa et al (2000) en Brasil (38%), Rodríguez Vivas et al (2001) en México (41%), Pinilla et al (2005) (62.5 %) y Cazorla Perfetti et al (2013) (29%) en Venezuela, pero fueron menores las reportadas por Ngowi et al (2014) (11,6%), Jufare et al (2015) (12%) y Atawalma et al (2016) (14,5%), en Tanzania, Ethiopia y Ghana, respectivamente, en similares sistemas de producción. La prevalencia de coccidios reportada por Descarga et al (2010), en sistemas de producción a campo de Argentina fue variable, entre 17 y 100%, y 40% en estudios preeliminares de Algañaraz et al (2016).
La variabilidad de resultados reportados en investigaciones de coccidios en cerdas reproductoras y los altos valores de prevalencia hallados, plantean el desafío para desarrollar estudios futuros en sistemas de producción de cerdos a campo específicamente evaluando el impacto en la producción.
Conclusiones
La elevada prevalencia de los helmintos gastrointestinales en cerdos criados en sistemas al aire libre debe ser tenida en cuenta para implementar estrategias tendientes a la aplicación de mejoras en el manejo sanitario, nuevas medidas de control y prevención y evitar la presentación de resistencia a drogas antiparasitarias de uso frecuente.
Los reportes acerca de la prevalencia de parásitos en SAL son escasos, y considerando la relevancia de los mismos para muchos países en desarrollo, es importante contar con información básica acerca de los parásitos predominantes y de aquellos que pueden ser causa de enfermedad zoonótica.
Bibliografía
- ALGAÑARAZ, F.; BELANDO, M.; CARDILLO, N.; MATASSA, M.; TOSONOTTI, N.; RONCORONI, A.; SCIARROTTA, R. y col. 2016. Prevalencia de helmintos gastrointestinales en producciones porcinas al aire libre. Memorias XII Congreso Nacional de Producción Porcina VIII Congreso de Producción Porcina del Mercosur. ISBN 978-987-688-177-7.p.
- ATAWALNA, V. ATTOH-KOTOKU, R.D. FOLITSE1, C. AMENAKPOR. Prevalence of Gastrointestinal Parasites among Pigs in the Ejisu Municipality of Ghana. Sch J Agric Vet Sci., Dec-2015-Jan 2016; 3(1):33-36
- BURDEN DJ, HAMMET NC, BROOKES PA. 1987. Field observations on the longevity of Trichuris suis ova. Vet Rec (121): 43.
- CARSTENSEN L., VAARST M., ROEPSTORFF A. 2002. Endoparasite infections in Danish organic swine herds. Vet Parasitol; (106): 253–264.
- CAZORLA PERFETTI, S.; ACOSTA QUINTERO, M.; TORTOLERO LOW, J.; MORALES MORENO, P. 2013. Prevalencia de enteroparásitos porcinos en una comunidad rural de la Península de Paraguaná, Estado Falcòn, Venezuela. Revista Científica, FCV-LUZ/Vol.XXIII, Nº1, 19-25
- CORWIN RM, STRAW B. Parásitos internos en: STRAW B, D’ALLAIRE S, MENGELING WL, TAYLOR D. 2001. Enfermedades del cerdo. 8ª edición. Editorial Intermédica.: 599-614.
- DALLA COSTA O.; MORÉS, N.; PEDROSO-DE-PAIVA, D.; SILVA, R.; SOBESTIANSKY, J.; CICERO, J. y col. 2000. Acompanhamento parasitário de rebanhos suínos no sistema intensivo de suínos criados ao ar livre – siscal. Embrapa Suínos e Aves, Comunicado técnico. Nº 253. Setembro/, p. 1–3.
8. DESCARGA, C.; COTTURA, G.; FRANCO R, BRUNORI J, URBANI L, SPINER N, PANICHELLI D. 2010. Dinámica de huevos de nematodes gastrointestinales y de ooquistes de coccidios en heces de cerdos de recría-terminación durante dos años de uso de una pastura de cobertura. Memorias del X Congreso Nacional de Producción Porcina, Mendoza, Argentina. p. 282.
Disponible en: https://es.slideshare.net/diananp7/prevalencia-y-anlisis-molecular-de-ascariosis-en-porcinos-y-humanos-en-comunidades-rurales-del-estado-de-guerrero-mxico.
- EIJCK IA, BORGSTEEDE FH. 2005. A survey of gastrointestinal pig parasites on free-range, organic and conventional pig farms in The Netherlands. Vet Res Commun; 29(5):407
- GARCÍA-VALLEJO T. Endoparasitosis del porcino ibérico en Extremadura (España): epidemiología y control. Universidad de Extremadura. Cátedra de Parasitología, Enfermedades Parasitarias, Medicina Preventiva y Policía Sanitaria. Disponible en: http://biblioteca.unex.es/tesis/8477234140.PDF
- HAUGEGAARD J. 2010. Prevalence of nematodes in Danish industrialized sow farms with loose housed sows in dynamic groups. Vet Parasitol; (168): 156- 159.
- JUFARE A, AWOL N, TADESSE, F, TSEGAYE Y, BIRHANU H. 2015. Parasites of pigs in two farms with poor husbandry practices in Bishoftu, Ethiopia. Onderstepoort Journal of Veterinary Research 82(1), http://dx.doi.org/10.4102/ojvr.v82i1.839
- JENSEN TK, SVENSMARK B. Trichuriasis hos udendørs slagtesvin. Vet Inform 1996; (2): 3–7.
- LUNA L, KYVSGAARD N. 2005. Ocho diferentes especies de parásitos gastrointestinales fueron identificadas en cerdos de traspatio en El Municipio de El Sauce - León. Nicaragua. REDVET ISSN 1695-7504.. http://www.veterinaria.org/revistas/redve
- NGANGA CJ, KARANJA DN, MUTUNE MN. 2008. The prevalence of gastrointestinal helminth infections in pigs in Kenya. Trop Anim Health Prod. Jun;40(5):331-4.
- NEJSUM P, PARKER ED JR, ROEPSTORFF A, BOES J, HAQUE R, et al. Ascariasis Is a Zoonosis in Denmark. 2005. J Clin Microbiol, 43(3):1142-1148.
- NGOWI1 HA , CHENYAMBUGA S, SAMBUTA A, MKUPASI E, CHIBUNDA R, 2014. Co-endemicity of cysticercosis and gastrointestinal parasites in rural pigs: a need for integrated control measures for porcine cysticercosis. Sci Parasitol 15(1-4):1-10.
- NOLASCO PD, MARTINEZ MJ, SCHUNEMANN AD, PERALTA, GEA, MARTINEZ, MMG, RODRIGUEZ AC, PONCE MM. 2013. Prevalencia y análisis molecular de ascariosis en porcinos y humanos en comunidades rurales del Estado de Guerrero, México. Conferencia XXI Congreso Latinoamericano de Parasitología. Guayaquil- Ecuador.
- PINILLA JC, DASILVA N, GONZALEZ C, TEPPER, R. 2005. Prevalencia e intensidad de infección de parásitos gastrointestinales en cerdos alojados en diferentes sistemas de producción. Rev Unell Cien Tec; (23) : 51-61.
- RODRÍGUEZ VIVAS, L.; A ORTEGA PACHECO, C.; MACHAIN, W. Y SANTOS RICALDE, R. 2001. Parásitos gastrointestinales en marranas mantenidas en dos sistemas de producción (interior y exterior) en el trópico mexicano Livestock Research for Rural Development 13 (5)
- ROEPSTORFF A, MEJER H, NEJSUM P, THAMSBORG SM. 2011. Helminth parasites in pigs: new challenges in pig production and current research highlights. Vet Parasitol; 180 (1-2):72–81.
- ROESEL1 K, DOHOO I, BAUMANN M, & DIONE M, GRACE D, CLAUSEN PH. 2017. Prevalence and risk factors for gastrointestinal parasites in small-scale pig enterprises in Central and Eastern Uganda. Parasitol Res (2017) 116:335–345
23. Servicio Nacional de Sanidad y Calidad Agroalimentaria (SENASA). 2016. Disponible en http://www.senasa.gob.ar/cadena-animal/porcinos
- THAMSBORG SM, ROEPSTORFF A, NEJSUM P, MEJER H. 2010. Alternative approaches to control of parasites in livestock: Nordic and Baltic per- spectives. Acta Vet Scand; 52 (1): 1–5.
- VÁZQUEZ MR, TIRANTI K, CHIARETTA A, LARRIESTRA K. 1997. Dinámica de las infecciones helmínticas y su influencia en la ganancia de peso en cerdos criados al aire libre. Memorias de VII Congreso Latinoamericano de veterinarios especialistas en cerdos y V Congreso Nacional de Producción Porcina. Argentina. p. 116.
- ZEWDNEH T, IMAM E, KIFLEYOHANNES T, TEKLE I, WELDU K. Prevalence of gastrointestinal parasites and Cryptosporidium species in extensively managed pigs in Mekelle and urban areas of southern zone of Tigray region, Northern Ethiopia. Veterinary World; 6(7):433.
- ZEWDNEH, T., EKWAL, I., TSEGABIRHAN, K., YOHANNES, T. & KIDANE, W., 2013, ‘Prevalence of gastrointestinal parasites and Cryptosporidium in extensively managed pigs in Mekelle and urban areas of southern zone of Tigray region, Northern Ethiopia’, Veterinary World 6(7), 433–439. http://dx.doi.org/10.5455/ vetworld.2013.433-439
- ZHOU C, LI M, YUAN K, DENG S, PENG W. 2012. Pig Ascaris: an important source of human ascariasis in China. Infection, genetics and evolution. Journal of molecular epidemiology and evolutionary genetics in infectious diseases. 12(6), pp.1172–1177. Available at: http://www.ncbi.nlm.nih.gov/pubmed/22561394 [Accessed October 13, 2013]
Agradecimientos:
Universidad Nacional de Luján quien financió el estudio.
Productores propietarios y empleados que permitieron y colaboraron en los trabajos de campo.











